 川公网安备51019002008863
川公网安备51019002008863
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息

全球数据
开放手术一直是严重三尖瓣疾病(如三尖瓣反流 (TR))的主要治疗方法。
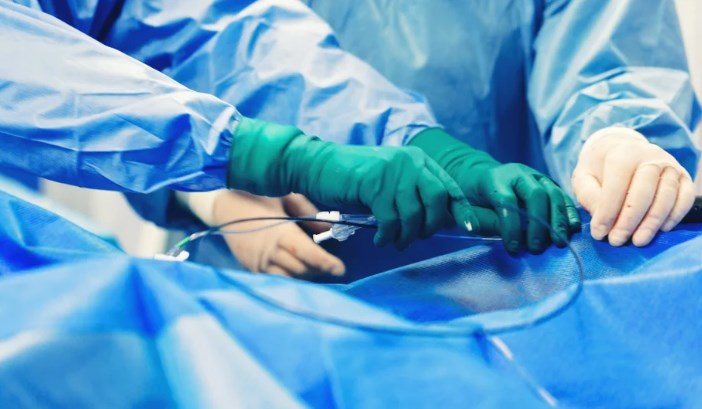
同时,这些患者通常不适合接受手术治疗——表现出严重 TR 的患者通常年龄较大,因此由于高龄和合并症而被认为是高风险的。
Edwards Lifesciences 推出的微创经导管三尖瓣置换术 (TTVR) 系统 EVOQUE 为这些人提供了一种接受 TR 治疗的替代且更安全的方式。
EVOQUE TTVR 系统于 2023 年 10 月获得 CE 批准,并于本月早些时候获得美国食品和药物管理局 (FDA) 的批准。
该装置是目前唯一可用于治疗严重 TR 的经导管疗法。
GlobalData 称,到 2033 年,EVOQUE 系统的批准将极大地促进 TTVR 市场的预期积极增长,达到 20 亿美元以上。
Edwards Lifesciences 对 TTVR 市场的垄断并没有阻止其他公司试图进入该市场。
特别是,自 2020 年获得 FDA 突破性认定以来,美敦力仍在对其 Intrepid 系统在重度 TR 患者中的早期可行性研究。
德国、瑞士、法国、美国和日本等拥有响应迅速的监管和报销机构的国家预计将观察到 15-25% 的采用率,而英国、西班牙和意大利等采取更谨慎方法的国家可能会看到 3-8% 的增长率。
然而,印度等发展中经济体的国家可能会看到1-3%的增长率。
采用 TTVR 的障碍包括设备成本高昂和外科医生缺乏 TTVR 植入手术的培训。
虽然 EVOQUE 系统等经导管设备为接受 TTVR 治疗提供了更安全、风险更低的替代方案,但治疗重度 TR 患者仍存在大量未满足的临床需求,尤其是在发展中国家。
•
•
•
•
•
•
•
•
•
•